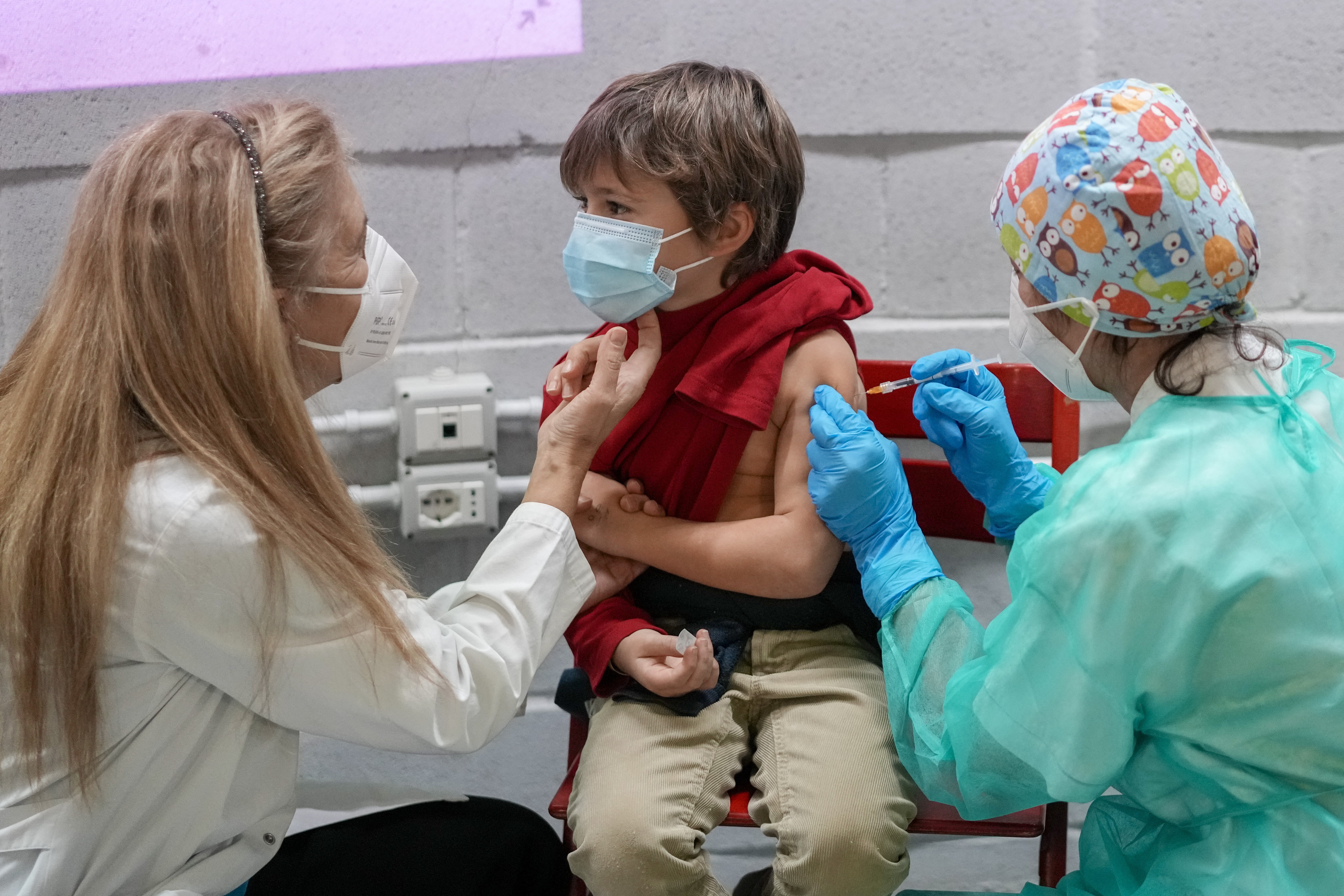
Inclusão de grupo no programa de imunização ainda depende da chegada de doses específicas. Menino recebe dose da vacina da Pfizer contra a Covid-19 em Roma, na Itália Andrew Medichini/AP Após a Anvisa anunciar que liberou a vacinação contra Covid-19 com o imunizante da Pfizer para crianças com idades entre 5 e 11 anos, a Secretaria Estadual de Saúde Pública do Rio Grande do Norte (Sesap) estimou que a imunização desse público no estado só deve começar em janeiro de 2022, após a chegada de doses específicas. De acordo com a coordenadora da Vigilância em Saúde, o estado tem cerca de 350 mil crianças nessa nova faixa etária a ser incluída no programa de imunização. "Julgamos que é importante a ampliação da vacinação para esse público, porém a gente espera que os imunizantes cheguem em tempo oportuno. O Ministério da Saúde já sinalizou que não tem esse quantitativo de imunizantes para iniciar a vacinação desse público ainda em 2021", afirmou. LEIA TAMBÉM: Veja o que está em prática no mundo O que se sabe sobre vacina contra Covid-19 em crianças no Brasil "Nós acreditamos que exatamente por essa deficiência no número de doses, que ainda não chegaram aos estados, esse início só se dará em janeiro do próximo ano", completou. Ainda de acordo com ela, por se tratar do público infantil, as doses serão menores, e por isso o estado não poderia usar as vacinas já em estoque. Também é necessário esperar as orientações técnicas do Ministério da Saúde sobre o assunto. Apesar disso, Kelly acredita que o público irá atender à convocação para a imunização. "É uma faixa (etária) que tem o hábito de ser vacinada, até pela caderneta de imunização. Quando as doses chegarem, prontamente iremos fazer a distribuição e as orientações aos municípios", pontuou. Anvisa libera uso A Agência Nacional de Vigilância Sanitária (Anvisa) autorizou nesta quinta-feira (16) a aplicação da vacina da Pfizer contra Covid-19 em crianças de 5 a 11 anos. Ainda não há previsão de quando a imunização vai começar porque a vacina para este público tem diferenças em relação a que foi aplicada nos adultos. Por isso, o governo federal terá que comprar uma versão específica do produto com dosagens e frascos diferentes (foto acima), apesar de o princípio ativo ser o mesmo. A mesma autorização de uso já foi concedida pelo FDA e pela EMA (agências regulatórias de saúde dos Estados Unidos e União Europeia), além de países como Costa Rica, Colômbia, República Dominicana, Equador, El Salvador, Honduras, Panamá, Peru e Uruguai. Versão pediátrica A dose para as crianças entre 5 e 11 anos de idade é 1/3 da formulação já aprovada no Brasil. A formulação pediátrica é diferente daquela aprovada anteriormente apresentada para o público com mais de 12 anos – portanto, não pode ser utilizada a formulação de adultos diluída. A criança que completar 12 anos entre a primeira e a segunda dose deve manter a dose pediátrica. Também participaram da avaliação especialistas das sociedades brasileiras de Infectologia (SBI), de Imunologia (SBI), de Pediatria (SBP), de Imunizações (SBIm) e de Pneumologia e Tisiologia. "Mesmo que seja um público que representa poucos casos de Covid-19, quando a gente faz um recorte, tem morrido mais crianças com covid-19 do que com outras doenças que são prevenidas com vacina, como o sarampo. Por isso a importância dessa imunização, além de a criança ser um vetor de transmissão. Embora a vacina não tenha cessado a transmissão entre adultos, pode ser que tenha esse efeito nas crianças", ponderou a imunologista Janeusa Souto, que é professora da Universidade Federal do Rio Grande do Norte.


0 Comentários